Treg-免疫抑制T细胞研究进展
调节性T细胞(Tregs)是由具有抑制免疫反应能力的T淋巴细胞组成的异质性群体,其中CD4+Foxp3+Tregs研究最多。它们通过抑制T效应细胞(T effs)的功能促进癌症的发生和发展。在大多数癌症类型中,肿瘤内CD8+T细胞与Tregs的比值降低与预后不良有关。Tregs在建立和维持免疫抑制的肿瘤微环境(TME)以抑制抗肿瘤免疫方面发挥关键作用。
有研究表明,肿瘤中的PD-1信号可以抑制T effect细胞的功能和维持肿瘤中Treg亚群,PD-1/PD-L1轴可能影响Treg的分化和功能,如:PD-1通过增加FoxP3的表达来增加Tregs的稳定性。PD-1/PD-L1单克隆抗体的应用通过增加T effs细胞的活性来增强对肿瘤的抑制,从而减弱Treg抑制。
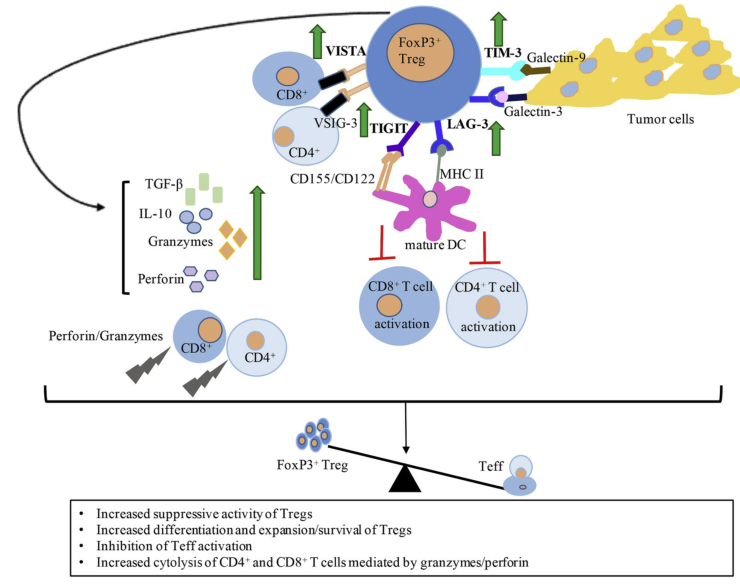
Treg本身也可以产生大量的TGF-β,进而通过促进成纤维细胞转化为CAF来诱导CD8+T细胞凋亡,从而促进肿瘤对细胞毒性T细胞的逃逸,TGF-b被认为是肿瘤微环境内重要的抑制性细胞因子,TGF-β也可以反馈促进Tregs的存活。TGF-β也通过诱导MDSC等免疫抑制细胞分化,进而诱导Tregs的产生,除此之外,Treg可以通过分泌IL-10诱导单核细胞分化为TAMs(具有免疫抑制表型的M2巨噬细胞)。这表明Tregs是参与TME内的免疫抑制网络的重要角色。
肿瘤细胞在缺氧条件下可以分泌高水平的CCL28,这一趋化因子可以将 Tregs招募到TME ,有趣的是Tregs可以在低氧条件下存活。基于这一知识,有研究认为由于缺氧,TME肿瘤内的Tregs变得更加具有免疫抑制性并产生对PD-L1mAb治疗的耐药性。
此外,有研究结果显示,CD73的表达与黑色素瘤患者的不良预后呈正相关。对PD-1 mAb产生获得性耐药的黑色素瘤患者也显示了CD73表达上调。Foxp3+Tregs可诱导腺苷介导的免疫抑制途径,该途径涉及胞外酶CD39和CD73。NT5E(编码CD73的基因)在Tregs中的表达上调影响了T effs的激活/增殖及相关细胞因子的释放。阻断ICs结合抑制CD73的临床试验正在进行中(NCT02503774)。
例如下图,我们通过Indica HALO软件的Tissue classify 功能区分肿瘤实质和间质,并可以统计实质和间质内的CD8+T,CD4+T和CD4+foxp3+Treg的比例;这个panel中我们还结合了PD-1染色,我们发现除了浸润入肿瘤实体的激活和耗竭的 CD4+ 和 CD8+ T 细胞表达有PD-1,Treg 同样表达有 PD-1。因此,PD-1 阻断剂对实体瘤的作用便不能简单描述为增强肿瘤浸润杀伤 T 细胞功能进行杀瘤。PD-1 阻断剂对瘤内浸润 Treg 细胞的作用机制如何,造成何种临床结果便成了需要回答的核心问题,对深入了解复杂的肿瘤微环境并进行有效调控提出更高的要求。

五标(PanCK、Foxp3、CD8、CD4、PD-1)六色全片扫描
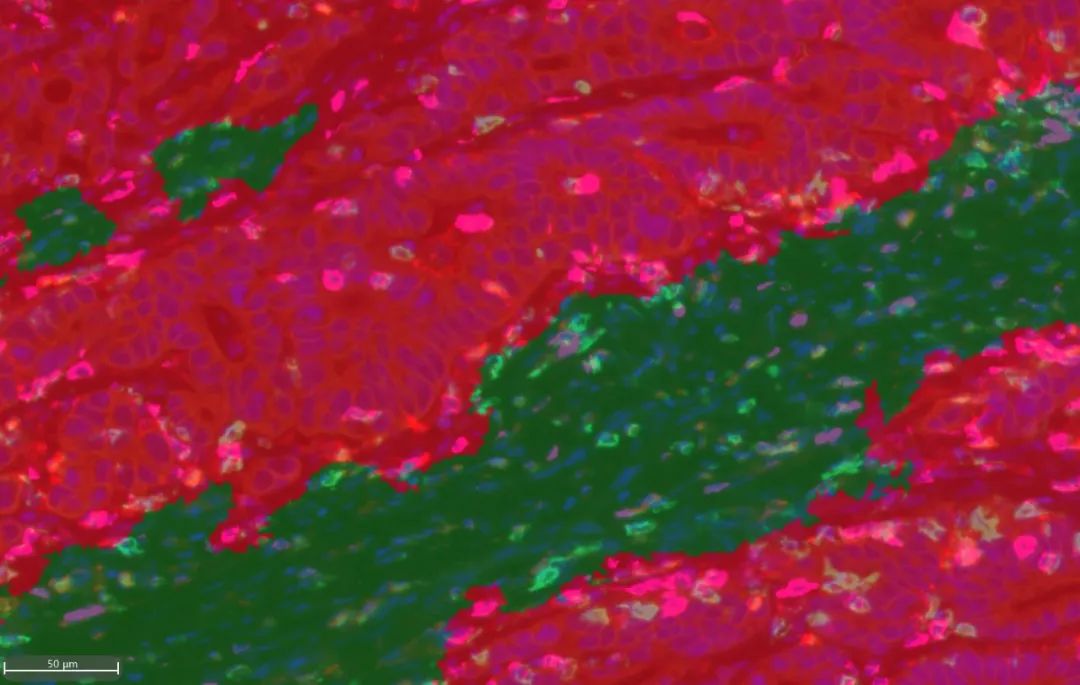
肿瘤实质,间质区分(Indica Halo tissue classify 功能模块)

媛禧生物是一家专注于组织水平biomarker定量检测、分析的CRO公司。
我们聚焦抗肿瘤新药研发过程中的现实难题,采用先进技术,利用本土生物样本资源优势,帮助新药研发企业在靶点研究、药物作用机制、临床转化和伴随诊断方案开发领域提供专业的技术服务。



